人工智慧技術 預測腦癌病患的治療結果
斯坦福大學(Stanford University)的醫學院研究團隊,透過利用400多名膠質母細胞瘤患者的空間轉錄組圖像(Spatial Transcriptomics)和遺傳數據進行模型的訓練,成功開發一模型'GBM36',指出該模型可以藉由評估膠質母細胞瘤組織的染色圖像,預測患者腫瘤的侵襲性,確定腫瘤細胞的基因組成,幫助外科醫生了解大腦中可能殘留有多少癌細胞,以及手術後多久才能恢復治療。
膠質母細胞瘤 難以治療的腦癌
膠質母細胞瘤是一種極具挑戰性的腦腫瘤,一直以來都令醫學界和患者面臨極大的困難。“由於這種疾病的異質性,科學家們還沒有找到解決它的好方法。”,斯坦福大學的生物醫學信息學和數據科學副教授,Olivier Gevaert博士說。
並且由於很難分辨哪些惡性細胞驅動了患者的膠質母細胞瘤,在預後的方面,醫生以及科學家也面臨挑戰。
但斯坦福醫學院的科學家團隊最近開發了一個人工智慧模型,該模型評估了膠質母細胞瘤組織的染色圖像,以預測患者腫瘤的侵略性、確定腫瘤細胞的基因組成,並評估手術後是否仍有大量惡性細胞存在。
“這在某種程度上是為醫生提供的決策支持系統。”, Gevaert 實驗室的博士後研究學者Yuanning Zheng博士說道。
AI協助 膠質母細胞瘤新觀點
膠質母細胞瘤患者復發的機率極高,即使患者經歷手術、放射線治療和化療,仍然幾乎總會有一些癌細胞殘留。
醫生和科學家通常使用稱為組織學圖像(histology images)或已染色疾病組織的圖片,以幫助他們識別腫瘤細胞並制定治療計劃。儘管這些圖像通常揭示了癌細胞的形狀和位置,但它們並不能完整呈現腫瘤的全貌。近年來,出現了一種更高級的技術,稱為空間轉錄組圖像(spatial transcriptomics)。它利用特定分子來識別腫瘤組織中的基因物質,顯示了數十種細胞類型的位置和基因組成。然而,此技術需花費非常龐大的金額,單個患者需數千美元來生成數據;
因此,Gevaert 和 Zheng 轉向人工智慧來節省成本,開發了一個模型,利用空間轉錄組圖像數據並增強基本的組織學圖像,從而創建更詳細的腫瘤訊息。
“這個模型顯示了哪些細胞喜歡在一起,哪些細胞不希望互相往來,以及這如何與患者的結果相關,” Gevaert 說。
人工智慧 腫瘤預防與判斷更精準有效
研究人員對這個模型進行了訓練,使用了來自20多名膠質母細胞瘤患者的空間轉錄組學圖像和基因數據。從這些詳細的圖像中,可以瞭解哪些細胞類型、細胞間的互動以及特定特徵與較有利(或不利)的癌症結果相關。
例如,模型發現,當與神經元支持細胞相似的腫瘤細胞,稱為星形膠質細胞(astrocyte),在不正常情況下聚集在一起時,患者似乎患有更迅速、更具侵略性的癌症。其他研究發現,當星形細胞聚集在一起時,它們會傳達促使腫瘤生長的生物信號。
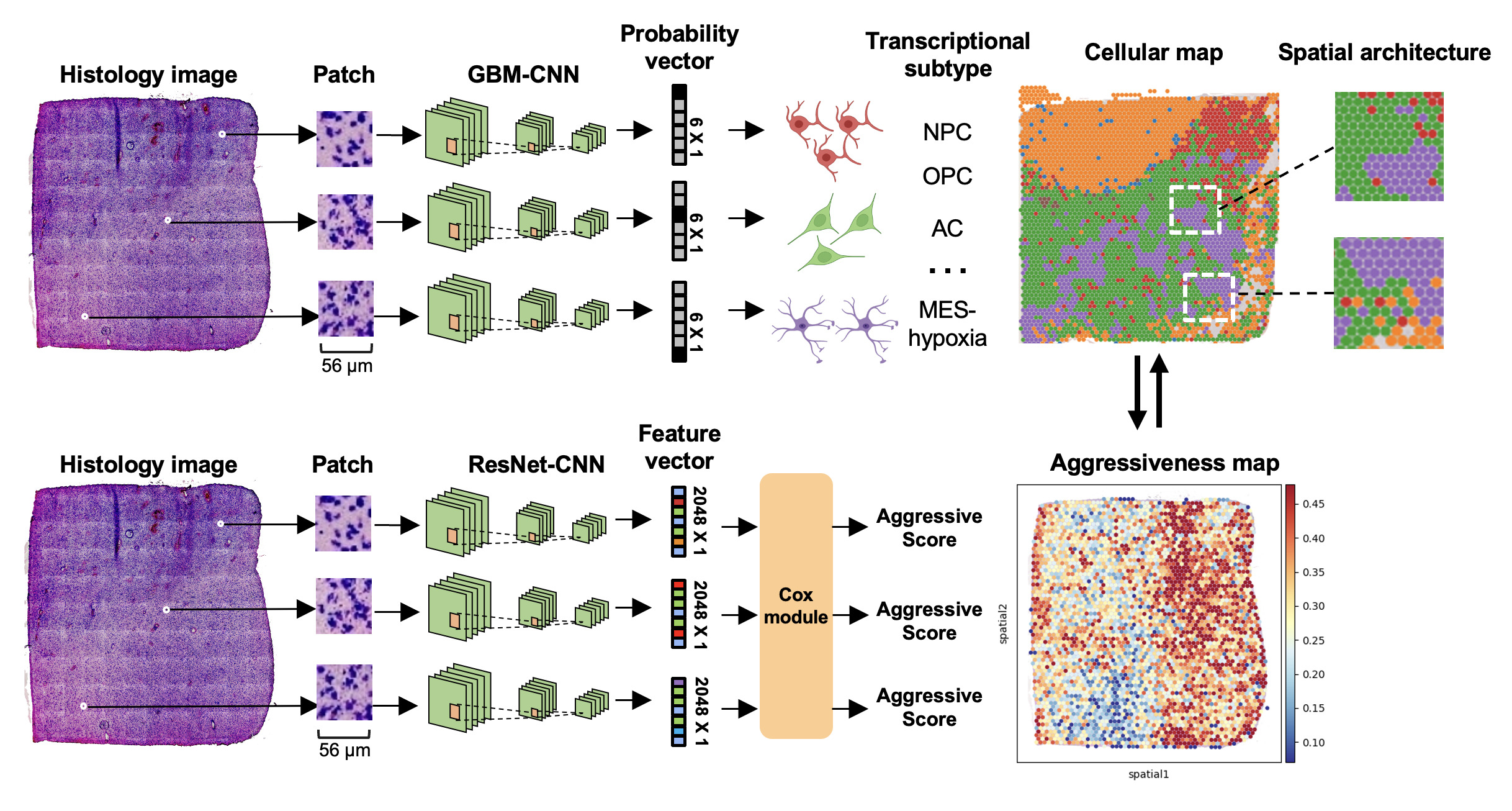
圖片來源:gbm360
通過顯示這種類似識別的細胞模式,該模型可能有助於藥物開發人員設計更有效的治療方法來針對膠質母細胞瘤,Gevaert表示。
來自同一膠質母細胞瘤患者的空間轉錄組學數據,還訓練了模型以高達78%或更高的準確度,識別相應組織學圖像中的不同腫瘤細胞。基本上,它使用細胞的形狀來預測哪些基因是“驅動”和“無關”的,這些信息揭示了細胞的身份。
利用此人工智慧,Zheng還希望可以協助臨床醫生來推斷手術中腫瘤成功切除了多少,以及腦內還剩下多少。他們的模型顯示,帶有帶有缺氧基因痕跡的腫瘤細胞(tumor cells with genetic traces of oxygen deprivation)通常位於患者腫瘤的中心。當這些細胞比例較高時,與之相對應的癌症結果更糟。通過在組織學染色的手術樣本中顯示缺氧細胞(oxygen-deprived cells),該模型可以幫助外科醫生了解腦內可能剩下多少癌細胞,以及手術後多久可以恢復治療,Zheng表示。
一旦模型被訓練來識別基本圖像中不同細胞類型的位置,研究人員在另一個包含410名患者組織學圖像的大型獨立數據集上評估了其效用。從這些圖像中,模型開始推斷癌症結果。研究人員發現,模型能夠識別與癌症侵略相對應的細胞模式。
研究團隊表示,該模型有朝一日可能幫助醫生識別那些具有表明腫瘤更具侵略性,並可能構成即時威脅(無論是復發還是迅速生長)的患者。
個人化醫學的一大進展
目前,該模型GBM360的概念驗證版本已經可供研究人員上傳診斷圖像,並預測膠質母細胞瘤患者的結果。不過,Zheng強調,該模型仍處於研究階段,算法的結果目前還不應該直接指導患者的護理。
Zheng希望這個算法有一天可以預測其他疾病的結果,比如乳腺癌或肺癌等。他表示:“我認為這些多模態的數據整合可以塑造未來個人化醫學的改進。”
編輯來源和事實核查:
1. GBM360
2.Spatial cellular architecture predicts prognosis in glioblastoma,Nature Communications,2023.07.11
3.Scientists employ AI to predict brain cancer outcomes,Stanford Medicine,2023.08.22